シリカゲルとは
ケイ酸のコロイド溶液※1 を凝固させてできた非晶質※2構造を持つ化成品です。水ガラス(ケイ酸ナトリウム水溶液)に酸を加えて製造する方法が一般的です。20世紀初頭に、潜水艦内部の乾燥を目的として、アメリカから量産が始まりました。
構造は多孔質構造で、その内部はコロイド粒子の凝集した粒子の間にできる様々な大きさの細孔※3 を持ちます。細孔の構造は三次元網目構造で表面近辺は大きな径の細孔が多く、内部になる程次第に径が小さくなる分布を示します。
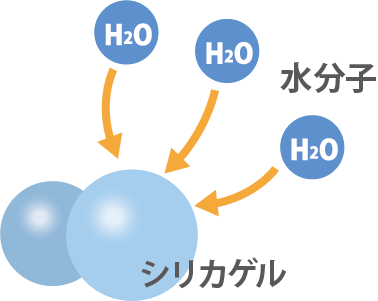
シリカゲルの組成は二酸化ケイ素(SiO2)が99%以上を占めます。この二酸化ケイ素は食品添加物にも指定される、不活性で安定した物質です。シリカゲルの凝集体の空間は小さいものから順にマイクロ孔、メソ孔、マクロ孔で構成されます。シリカゲルの表面はO原子やOH基が多数存在し、水やそのほかの極性物質を選択的に吸着します。水分に対して吸着能力が低下したシリカゲルは、過熱することで再び能力が回復します。これはシリカゲルに付着していたH2Oが気相に戻るためで、これを脱着と呼びます。マイクロ孔に吸着した水は約110℃、マクロ孔では約150~170℃で脱着します。
シリカゲルに水をかけると粒子は激しく破砕します。その理由は、一次粒子間に水がはいりこむことで凝集収縮が進んだためです。
シリカゲルは大きな比表面積を持ち、細孔径の制御が可能であるところや耐熱性に優れることから触媒の担体やクロマト充填材として利用されます。また、マイクロサイズの微粉末シリカゲルの応用例として固結防止剤や香料の担体として食品に添加されています。この他に研磨剤,増粘剤、塗料のつや消し剤としても利用されています。
シリカゲルの製造工程
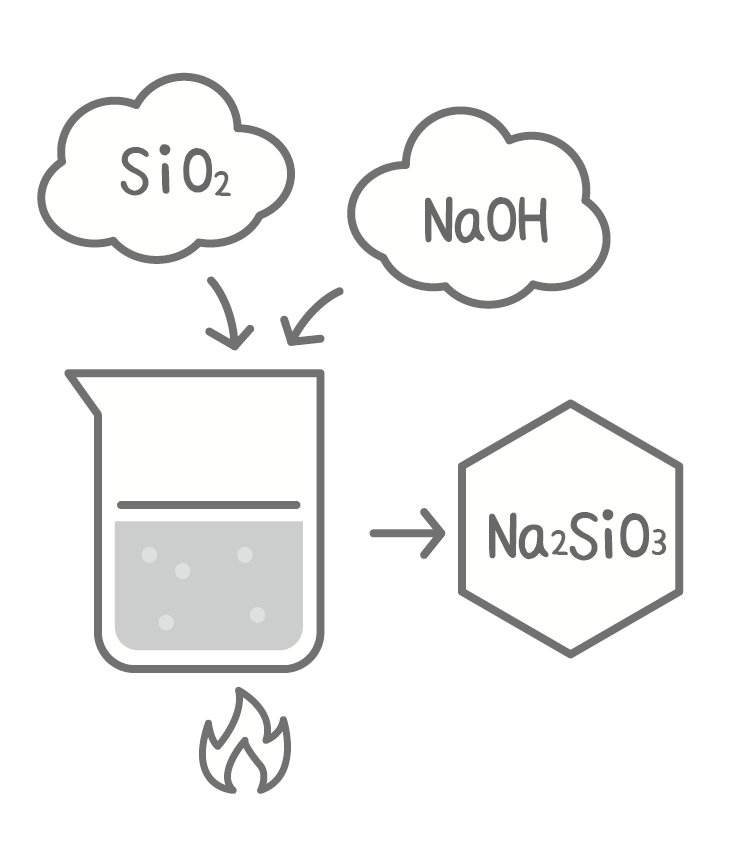
1.ケイ酸ナトリウムの生成
二酸化ケイ素(SiO₂)と水酸化ナトリウム(NaOH)を高温で反応させることで、シリカゲルの主原料となるケイ酸ナトリウム(Na₂SiO₃)が生成されます。
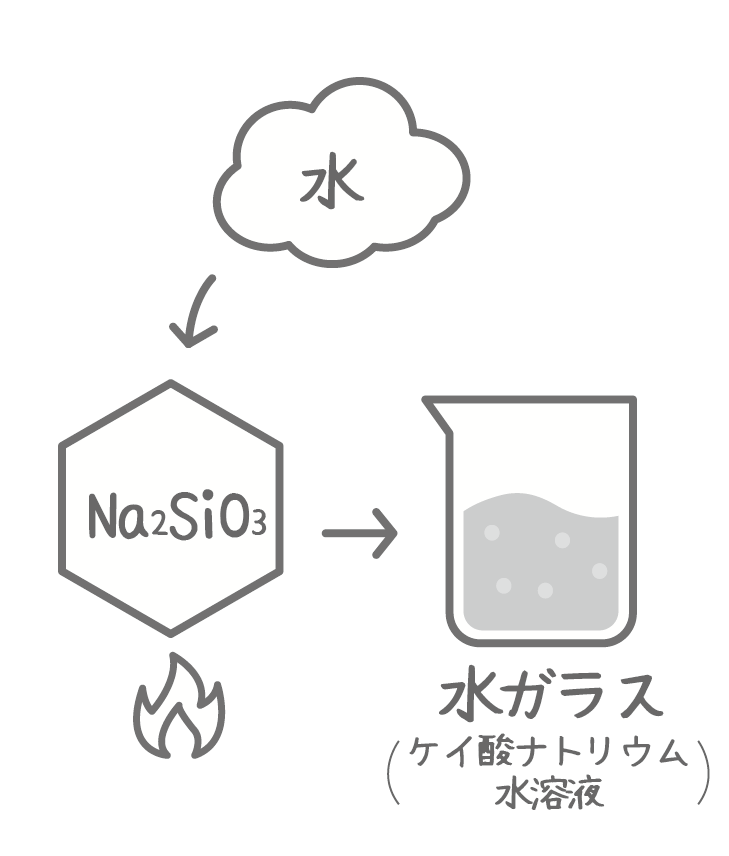
2.水ガラスの生成
生成したケイ酸ナトリウム(Na₂SiO₃)に水を加えて加熱などの処理を行うことで、成分が均一に混ざり合った粘り気のある液体になります。これが通称「水ガラス(ケイ酸ナトリウム水溶液)」と呼ばれる状態です。
この段階ではまだ液体(ゾル状)であり、次の工程で酸を加えることにより、反応が進みやすい状態が整います。
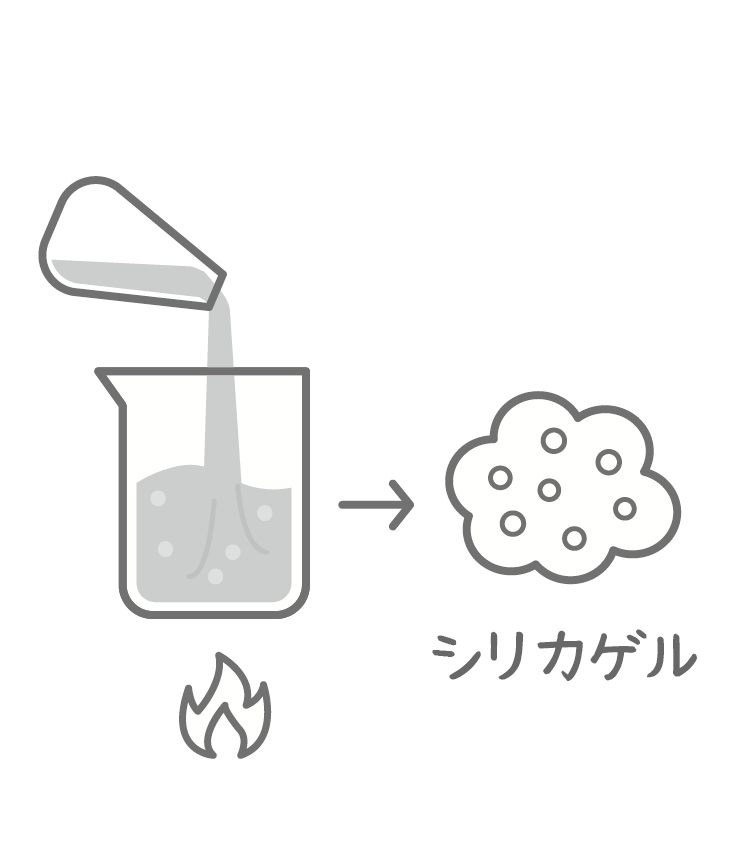
3.シリカゲルの生成
水ガラスに酸を加えるなどの適切な処理を行うと、溶液中のケイ酸成分が反応し、互いに結びついて網目状の構造を形成します。このとき、水分を多く含んだゼリー状の物質「含水シリカゲル(ヒドロゲル)」が生成されます。
その後、反応で生じた不要な不純物(塩分など)を水できれいに洗い流し、乾燥させます。乾燥によって水分が抜けると、内部に微細な孔(あな)をもつ多孔質構造が残り、強力な吸湿性をもつシリカゲルとなります。
| ※薬品の取り扱いや反応工程には専門的な知識と管理が必要です。一般の方が再現することを目的とした説明ではありません。 ※図は工程を概念的に説明したものであり、実際の反応や設備を正確に再現したものではありません。 | |||||||||||
シリカゲルの吸湿メカニズム
●A型シリカゲル
シリカゲルの吸着は表面上のシラノール基による科学的吸着減少と、木炭や活性炭と同様に水蒸気やガスなどの分子を強く固体表面に結合させる物理的吸着によるものがあります。大量の水蒸気を取り込む吸湿は後者(物理的吸着)の影響下にあり、微細な空間の表面積が乾燥剤としての性格を決めることになります。コロイド粒子間が密なことより、それぞれの 細孔の径が小さく、表面積がとりわけ大きいものをA型シリカゲルと呼びます。
低湿度時における水蒸気の吸着力に優れるため、食品、電子、精密部品など包装用乾燥剤として幅広く使用されます。
●B型シリカゲル
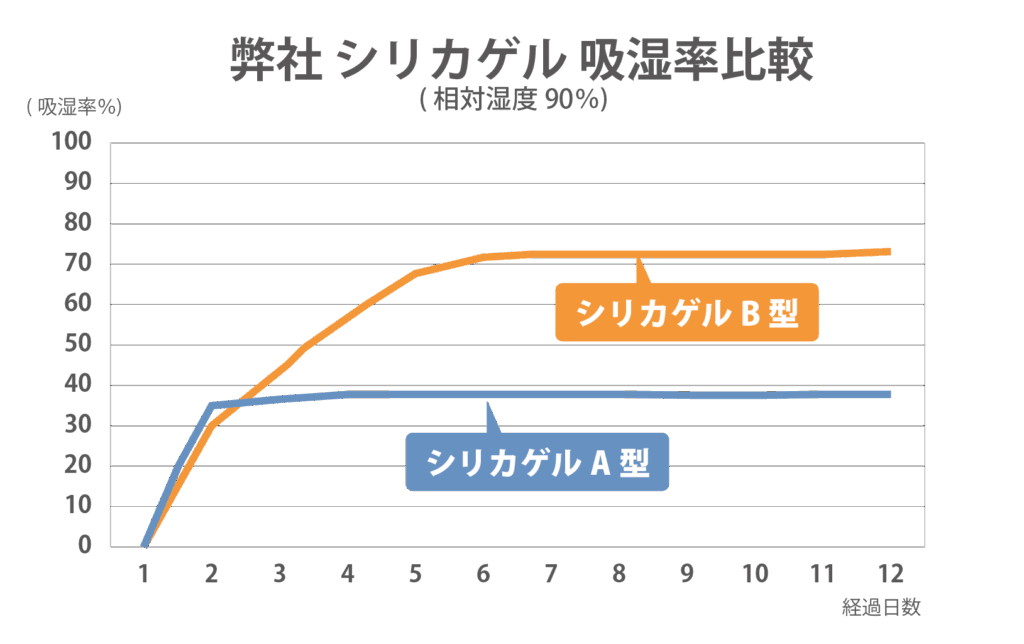
B型シリカゲルはA型シリカゲルに比べると、細孔の径をかなり大きく制御したものです。単位当たりの表面積は小さくなりますが、吸着等温線(下記グラフ参照)でもわかるように、関係湿度が高くなるに従い大量の水蒸気(ガス)を吸着する特長を持ちます。
同時に、常温でも関係湿度の低下により、保持した水蒸気(ガス)を吐き出す(脱着※6)緩慢な調湿作用により、高湿度時および乾燥状態での物性の変化を防ぐ働きをします。
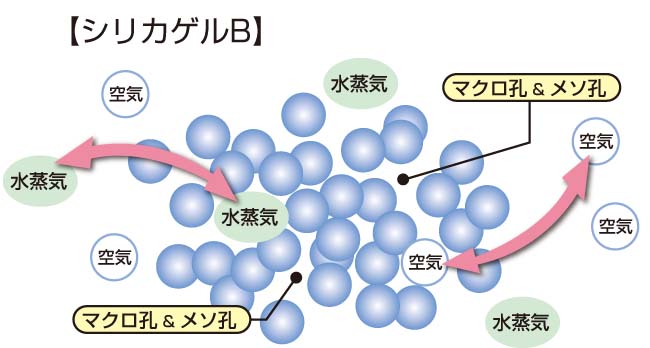
主な使途として床下調湿用、建築用、楽器用など、空間の雰囲気的湿度を調湿する目的で使用します。
※ 1 顕微鏡でも目に見えない、直径約10万分の1cm程の粒子が、水などの溶媒に溶けた溶液のこと
※ 2 原子の配列が規則的でなく、無秩序かつ不規則、またその表面は曲率の大きな凹凸状
※ 3 表面にはいろいろな形で凹凸ができるが、凸部の深さが直径より大きな孔を細孔と呼ぶ。
※ 4 ある固体の表面に、他の物質(分子やイオンなど)が結合して集まる現象
※ 5 主として物質の分散力に起因、ファン・デル・ワース吸着とも呼ばれる。結合力は分散力に依存するため比較的弱い。一方、化学的吸着は電荷移動や化学結合などを伴うもの。シリカゲルと異なり、塩化カルシウム、酸化カルシウム(生石灰)などが該当し、電子の授受による化学結合を結成するため結合力は非常に大きい。
シリカゲルと異なり、塩化カルシウム、酸化カルシウム(生石灰)などは化学的吸着による。
※ 6 吸着に対して脱着と呼ぶ。一度吸着したものが界面から離れることで吸着量も減る現象。
※ 7 JIS規格値は別紙グラフ参照
物理的吸着と化学吸着について
| 物理的吸着 | 化学吸着 | |
| 相互作用 | ファンデルワールス力 疎水性相互作用 | 共有結合、水素結合、イオン結合 |
| 吸着速度 | 速い | 遅い20 |
| 吸着速度の 温度係数 | 小 | 大(活性化エネルギー) |
| 可 逆 性 | 可逆性あり | 不可逆の場合もあり |
| 選 択 性 | なし | あり |
| 吸 着 量 | 多分子層吸着 | 単分子層吸着 |
| 吸 着 熱 | 凝縮熱より少し大 | 化学的反応熱 (物理的吸着より大) |
| 吸着分子間 相互作用 | 引力 | 反発 |
シリカゲルの安全性
リカゲルは、化学的に安定した二酸化ケイ素(SiO₂)を主成分とするため、環境負荷が低く、安全性の高い乾燥剤として広く利用されています。
シリカゲルJIS規格基準
| 項 目 | JIS規格値 | ||
| A型 | B型 | ||
| 吸 湿 率 | 相対湿度 20% | 8以上 | 3以上 |
| 相対湿度 50% | 20以上 | 10以上 | |
| 相対湿度 90% | 30以上 | 50以上 | |
| 含 水 率 | 2以下 | 2以下 | |
| P H | 4~8 | 4~8 | |
| 比抵抗 (Ω・cm) | 3000以上 | 3000以上 | |

A型シリカゲルとB型シリカゲルの簡易比較一覧
| 項目 | A型シリカゲル | B型シリカゲル |
| 細孔の表面積 | 約700㎡/g | 約450㎡/g |
| 細孔の大きさ | 細かい | A型より大きい |
| 吸湿特性 | 低湿度時の吸湿力に優れる | 高湿度時に 多くの水蒸気を吸着 |
| 低湿度での性能 | ◎ 優れている | △ A型より劣る |
| 高湿度での性能 | △ B型より劣る | ◎ 優れている |
| 再生条件 | 150℃以上の高温が必要 | |
| インジケーター | 塩化コバルト保持の 青シリカゲルを使用 | - |
| 主な用途 | 食品包装、電子部品、精密部品、化学機器、医薬品などの湿害防止 | 楽器、船舶、 床下調湿用途 |
| 水溶性 | なし | なし |
| 腐食性 | なし | なし |
| 潮解性 | なし | なし |
乾燥剤の使用量 JIS-Z0301による求め方
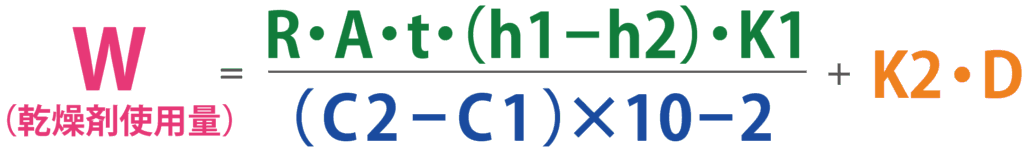
●K1の参考表
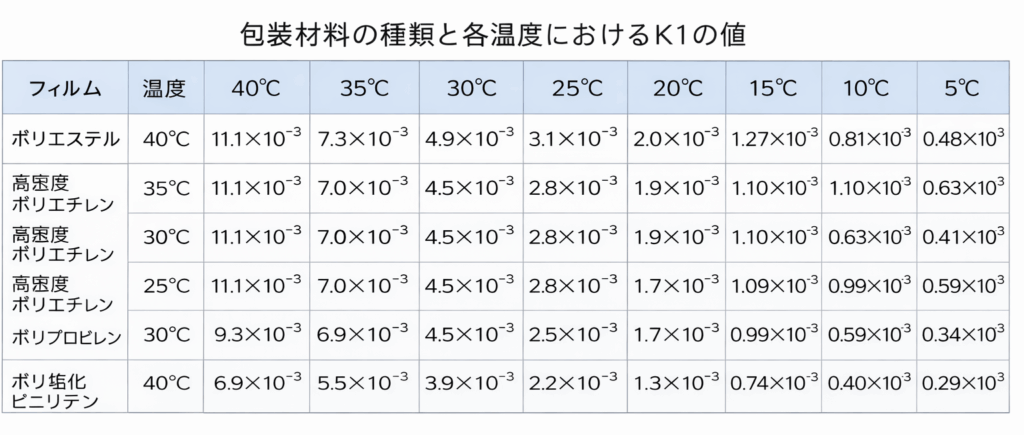

W:乾燥剤の使用量(g)
R:防湿包装材料(防湿フィルム等)の透湿度(g/㎡ 24h)
A:防湿包装材料(防湿フィルム等)の表面積 (㎡)
t:包装期間(輸送および保管する期間) (日)
h1:包装期間中の外気の平均湿度(%)
h2:包装期間中の包装内部の平均湿度 (%)
K1:包装材料の種類と、包装期間中の平均湿度によって定まる係数
C1:使用開始時の乾燥剤の吸湿率
C2:包装内部に許容される最高限度の相対湿度における乾燥剤の平衡吸湿率(%)
C3:包装内の許容される最高限度の湿度における吸湿性のある包装材料の平衡吸湿率(%)
C4:包装内に入れるときの吸湿性のある包装材料の平衡吸湿率(%)
K2:包装内の吸湿性のある包装材料の吸湿率によって定まる係数
D:包装内の吸湿性のある包装材料の質量 (g)
乾燥剤の使用量を正しく求めたいという方は
こちらにお問い合わせください↓

主なシリカゲル製品
- シリカゲル分包各種(A型)
- シリカゲル分包各種(B型)
- 業務用シリカゲル&活性炭 シリカーボン/シリカーボンPLUS
- 気化性防錆剤(VCI)
- 業務用除湿剤 ファインドライGシリーズ
- 除湿マットL判・L判PLUS
- Technos シリカゲルB型防湿シート
- 多機能シート TERA
- <住宅用>床下調湿剤・竹炭ゲル
- <工場・倉庫>ファインドライG大判プレート
- 炭ゲルマット 家庭用
- 炭ゲルマット 業務用
- <ピアノ調律師専用>防虫・防カビ剤 Dr.キーボー/Dr.キーボーII/ 1/2
- <ピアノ調律師専用>湿度調整剤
- ヘル臭バスター
- シュー臭バスターSPORTS
- シリカゲルシート(着物・衣類)
- 家庭用シリカゲル 万能乾燥剤
- さわやかシリカゲル
- きもの専用 除湿・消臭マット